MENU
CH | CHF
CH | CHF
-
- Toutes les centrifugeuses
- Centrifugeuses de paillasse
- Centrifugeuses au sol
- Centrifugeuses réfrigérées
- Microcentrifugeuses
- Centrifugeuses polyvalentes
- Centrifugeuses haute vitesse
- Ultracentrifugeuses
- Concentrateur
- Produits IVD
- Consommables pour centrifugeuses haute vitesse et ultracentrifugeuses
- Tubes à centrifuger
- Plaques de centrifugeuse
- Logiciel de gestion d’appareils
- Gestion des échantillons et des informations
-
- Pipettes, distributeurs et dispositifs de manipulation de liquides automatisée
- Pipettes mécaniques
- Pipettes électroniques
- Pipettes multicanaux
- Pipettes et distributeurs à déplacement positif
- Pointes de pipette
- Distributeurs sur flacon
- Auxiliaires de pipetage
- Accessoires pour pipettes et distributeurs
- Pipetage automatisé
- Consommables d’automatisation
- Accessoires d’automatisation
- Services pour pipettes et distributeurs
Sorry, we couldn't find anything on our website containing your search term.
Sorry, we couldn't find anything on our website containing your search term.

Protocole d’ensemencement cellulaire – guide pour réussir l’ensemencement
Lab Academy
- Biologie cellulaire
- Culture cellulaire
- Le quotidien au labo
- Pipetage et distribution
- Reproductibilité
- Pipettes
- Pointes de pipette
- Test
L’ensemencement cellulaire est généralement l’étape initiale d’un protocole et une procédure standard pour les expériences impliquant des cellules. Un protocole correct et standardisé est un facteur essentiel pour obtenir des résultats reproductibles. La principale difficulté réside dans l’obtention d’un nombre comparable de cellules à chaque itération de l’expérience.
Cet article a été publié à l’origine dans « Inside Cell Culture » , la newsletter mensuelle destinée aux professionnels de la culture cellulaire. Pour plus d’articles intéressants sur les incubateurs à CO2 : consultez notre page « FAQ et ressources sur les incubateurs à CO2 » .
Dr. Jessica Wagener, spécialiste des applications de manipulation cellulaire chez Eppendorf
L’ensemencement cellulaire est généralement l’étape initiale d’un protocole et une procédure standard pour les expériences impliquant des cellules. Un protocole correct et standardisé est un facteur essentiel pour obtenir des résultats reproductibles. La principale difficulté réside dans l’obtention d’un nombre comparable de cellules à chaque itération de l’expérience. Les variations du nombre de cellules ensemencées, ainsi que la formation de bulles d’air lors de l’ensemencement, augmentent la déviation standard et réduisent la fiabilité des résultats. C’est pourquoi vous devez prendre en compte plusieurs facteurs pour établir un protocole adapté au sein de votre laboratoire.
Lors de l’ensemencement des cellules, par exemple depuis un tube de 15 mL vers une plaque multi-puits, le remplissage complet de tous les puits nécessite un certain temps. Peu importe si vous utiliser ici une pipette monocanal ou multicanaux, plus le processus est long, plus vos cellules vont se sédimenter dans le tube. Par conséquent, vous n’obtiendrez pas le même nombre de cellules d’un puits à l’autre si vous n’agitez pas la suspension cellulaire dans le tube ou le réservoir (cf. image 1).
Dr. Jessica Wagener, spécialiste des applications de manipulation cellulaire chez Eppendorf
Sommaire
- L’impact des protocoles d’ensemencement cellulaire standardisés
- Le facteur temps et la sédimentation des cellules
- Vidéo : Une technique de pipetage appropriée
- Formation de bulles d’air
- Vidéo : Éviter la formation de bulles d’air au cours de l’ensemencement cellulaire
- Adhésion homogène des cellules
- Comportement lié à la densité cellulaire
Pourquoi l’ensemencement des cellules constitue-t-il une étape cruciale dans toute expérience de culture cellulaire ?
L’ensemencement cellulaire est généralement l’étape initiale d’un protocole et une procédure standard pour les expériences impliquant des cellules. Un protocole correct et standardisé est un facteur essentiel pour obtenir des résultats reproductibles. La principale difficulté réside dans l’obtention d’un nombre comparable de cellules à chaque itération de l’expérience. Les variations du nombre de cellules ensemencées, ainsi que la formation de bulles d’air lors de l’ensemencement, augmentent la déviation standard et réduisent la fiabilité des résultats. C’est pourquoi vous devez prendre en compte plusieurs facteurs pour établir un protocole adapté au sein de votre laboratoire.
Le facteur temps dans les protocoles d’ensemencement cellulaire
Lors de l’ensemencement des cellules, par exemple depuis un tube de 15 mL vers une plaque multi-puits, le remplissage complet de tous les puits nécessite un certain temps. Peu importe si vous utiliser ici une pipette monocanal ou multicanaux, plus le processus est long, plus vos cellules vont se sédimenter dans le tube. Par conséquent, vous n’obtiendrez pas le même nombre de cellules d’un puits à l’autre si vous n’agitez pas la suspension cellulaire dans le tube ou le réservoir (cf. image 1). Lire la suite
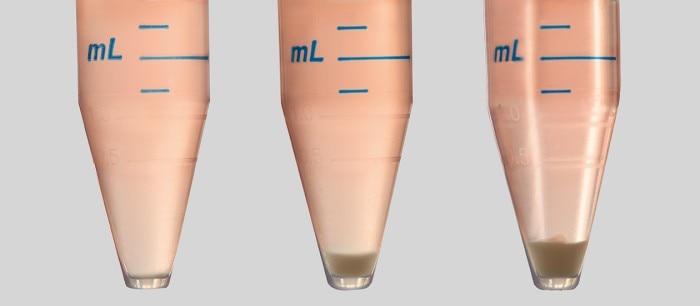
Image 1 : la sédimentation des cellules est un facteur clé à prendre en compte dans chaque protocole d’ensemencement cellulaire. Sédimentation des cellules dans le tube au bout de quelques minutes : plus l’ensemencement est long, plus le nombre de cellules baisse dans le surnageant.
Le processus de sédimentation des cellules est assez rapide (quelques minutes). Afin de prévenir cet effet, vous devez agiter ou remettre les cellules en suspension avant de les ensemencer pour assurer l’homogénéité de la solution. Ainsi, vous avez le même nombre de cellules par puits.
Vidéo : Une technique de pipetage appropriée dans un protocole d’ensemencement cellulaire
Lire la suite
Videos not loading, because cookies have been rejected. Change your

Formation de bulles d’air au cours de l’ensemencement
De la mousse a tendance à se former dans le milieu de la culture cellulaire en raison de la teneur élevée en protéine du sérum ajouté. Les bulles d’air empêchent l’attachement des cellules au cours de l’ensemencement, ce qui provoque des variations du nombre de cellules entre les puits (cf. image 2). Elles peuvent avoir un impact important, en particulier pour les petits formats de plaques (par ex. 96 et 384 puits), en raison de la faible surface de croissance par puits. Même si la remise en suspension ou l’agitation est nécessaire, faites attention à ne pas trop pipeter afin de minimiser la formation de bulles d’air. Un pipetage doux permet également de limiter l’exposition de vos cellules à des forces et au stress de cisaillement, un aspect essentiel de tout protocole d’ensemencement cellulaire.Lire la suite
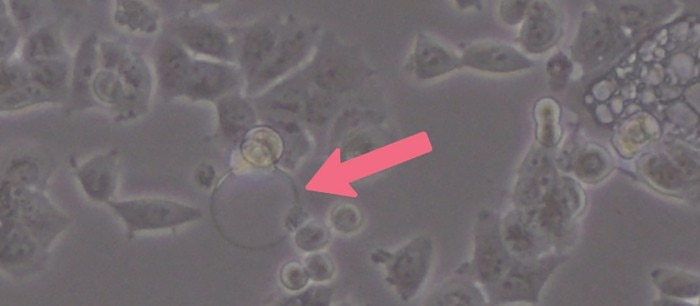
Image 2 : les bulles d’air formées au cours de l’ensemencement cellulaire peuvent nuire à l’adhésion des cellules. Observez que les cellules près de la bulle d’air présentent une adhérence insuffisante au fond du tube.
Vidéo : Éviter la formation de bulles d’air au cours de l’ensemencement cellulaire
Lire la suite
Videos not loading, because cookies have been rejected. Change your

Adhésion homogène des cellules
Au-delà du nombre total de cellules, une répartition homogène sur la surface de croissance d’un récipient de culture peut influencer le résultat de l’expérience. Plusieurs techniques sont couramment utilisées et sont généralement transmises par les chercheurs expérimentés à leurs apprentis. Mais quelle est la meilleure méthode pour répartir de manière homogène les cellules sur la surface de croissance ? Différentes techniques sont comparées sur l’image 3.À gauche, on observe ce qui se produit lorsque le récipient est simplement pré-rempli avec le milieu de culture avant l’ajout des cellules. Le résultat ? Les cellules adhèrent principalement au centre du récipient. Pour assurer une répartition homogène des cellules, certains procèdent en faisant un 8 alors que d’autres préfèrent un motif en croix sur la plaque ou la boîte. Ces deux techniques enregistrent une meilleure répartition des cellules que la première. Toutefois, plus le diamètre du récipient est petit, moins le liquide est mis en mouvement ce qui provoque une répartition inégale des cellules. Pour éviter cet effet lors de l’ensemencement, une méthode efficace consiste d’abord à diluer la suspension cellulaire dans un tube ou réservoir afin d’obtenir la concentration souhaitée (mastermix), puis à transférer le volume final dans le récipient de culture par pipetage.
Lire la suite
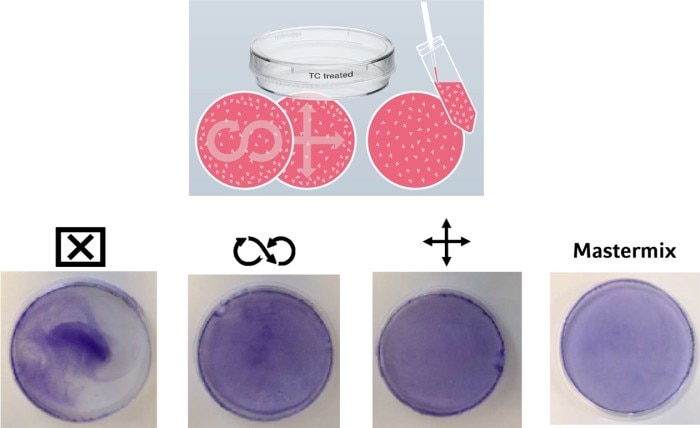
Image 3 : plusieurs méthodes présentant une efficacité variable existent. Elles ont toutes pour objectif d’assurer une adhésion uniforme des cellules après leur transfert dans le récipient de culture. Il est recommandé d’utiliser un mastermix avec la concentration finale de cellules. Du violet cristallisé a été utilisé pour fixer et colorer les cellules.
Quelle est l’importance de la densité cellulaire ?
L’homogénéité dans la répartition des cellules peut influencer de manière significative vos résultats expérimentaux. Bien entendu, tous les types de cellules ont tendance à croître en formant des colonies plutôt qu’une couche monomoléculaire homogène. Mais, en général, les cellules devraient se répartir sur toute la surface du récipient de culture de manière aussi homogène que possible. Un exemple de l’influence directe de la distribution et des réponses cellulaires est l’efficacité de la transfection (cf. images 4 et 5).Lire la suite
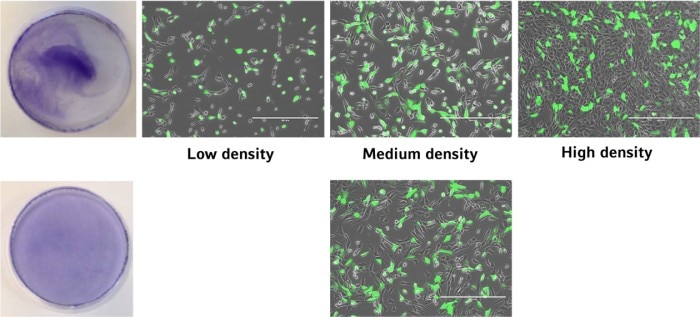
Image 4 : cellules transfectées à la GFP dans différentes zones d’une boîte de culture, après ensemencement réalisé avec deux méthodes distinctes.
Comme le montre le graphique, le taux maximal de cellules transfectées par rapport aux cellules non transfectées est obtenu à une densité cellulaire intermédiaire. De plus, une transfection efficace et homogène résulte d’une couche cellulaire uniformément répartie, obtenue grâce à la technique du mastermix. L’intégration de ces deux facteurs dans un protocole d’ensemencement cellulaire optimisera votre efficacité de transfection et réduira la déviation standard.
Lire la suite
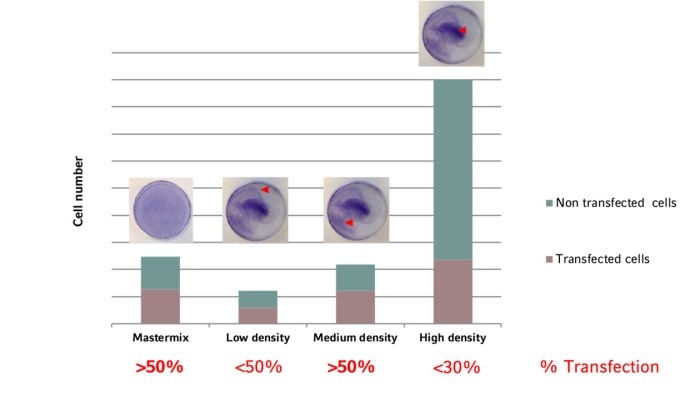
Image 5 : l’efficacité de transfection dépend de la densité cellulaire. Un taux de transfection optimal et une distribution homogène des cellules sont obtenus avec une densité cellulaire intermédiaire associée à la technique du mastermix.
