MENU
MA | EUR
-
-
-
- Services pour bioprocédés
- Services pour centrifugeuse et rotors
- Services pour Mastercycler
- Services pour automates de pipetage
- Services pour congélateurs
- Services pour incubateurs
- Services pour agitateurs
- Services pour appareils de photométrie
- Service de contrôle de la température et de l’agitation
- Service pour pipette
-
-
-
-
- Services pour bioprocédés
- Services pour centrifugeuse et rotors
- Services pour Mastercycler
- Services pour automates de pipetage
- Services pour congélateurs
- Services pour incubateurs
- Services pour agitateurs
- Services pour appareils de photométrie
- Service de contrôle de la température et de l’agitation
- Service pour pipette
-
MA | EUR
-
- Toutes les centrifugeuses
- Centrifugeuses de paillasse
- Centrifugeuses au sol
- Centrifugeuses réfrigérées
- Microcentrifugeuses
- Centrifugeuses polyvalentes
- Centrifugeuses haute vitesse
- Ultracentrifugeuses
- Concentrateur
- Produits IVD
- Consommables pour centrifugeuses haute vitesse et ultracentrifugeuses
- Tubes à centrifuger
- Plaques de centrifugeuse
- Logiciel de gestion d’appareils
- Gestion des échantillons et des informations
-
- Pipettes, distributeurs et dispositifs de manipulation de liquides automatisée
- Pipettes mécaniques
- Pipettes électroniques
- Pipettes multicanaux
- Pipettes et distributeurs à déplacement positif
- Pointes de pipette
- Distributeurs sur flacon
- Auxiliaires de pipetage
- Accessoires pour pipettes et distributeurs
- Pipetage automatisé
- Consommables d’automatisation
- Accessoires d’automatisation
- Services pour pipettes et distributeurs
Sorry, we couldn't find anything on our website containing your search term.
Vous vous apprêtez à quitter ce site.
Veuillez noter que votre panier actuel n’est pas encore enregistré et ne pourra pas être affiché sur le nouveau site ou lors de votre prochaine visite. Si vous souhaitez enregistrer votre panier, veuillez vous connecter sur votre compte.
Sorry, we couldn't find anything on our website containing your search term.

Flacons d’agitation – bien plus que des volumes de remplissage
Ines Hartmann Lab Academy
- Biologie cellulaire
- Culture cellulaire
- Mélangeurs et agitateurs
- Test
Les cultures agitées se développent dans des récipients spécifiques, aussi appelés flacons Erlenmeyer. Comparés à d’autres récipients de laboratoire, ces flacons se distinguent par une forme favorisant une agitation efficace tout en limitant les risques de débordement. Apprenez-en plus ici sur les formes et les matériaux, ainsi que leur influence sur l’aération.
Les bioréacteurs d’agitation, aussi appelés flacons Erlenmeyer ou simplement flacons d’agitation, ont vu le jour au début du siècle dernier. Disponibles dans une large gamme de volumes allant de 25 mL à 5 L, ils conviennent à de nombreux types d’expériences, telles que l’analyse et l’expansion, la préparation de milieux ou encore les étapes initiales de mise au point d’un procédé. Proposés à un prix avantageux, ils permettent de cultiver des bactéries, des levures et des champignons, ainsi que des cellules végétales et animales en suspension. Même si leur manipulation ne nécessite pas une formation spécifique, certains aspects sont à prendre en compte pour une culture efficace et pour choisir le bon type de récipient pour votre application.
Matériau : verre ou plastique
Les flacons existent en verre ou en plastique. Pour les applications classiques de microbiologie, les flacons Erlenmeyer en verre, réutilisables et autoclavables, conviennent généralement. Par ailleurs, lorsque le transfert d’oxygène est essentiel, ce matériau hydrophile favorise la formation du film liquide responsable du transfert d’oxygène. En comparaison, le plastique est hydrophobe, sauf traitement spécial [1]. Si toute contamination doit être évitée, par ex. lors de la manipulation de cultures sensibles ou d’étapes de production délicates, les flacons stériles à usage unique équipés d’un capuchon d’aération et d’un filtre de 0,2 µm garantissent une facilité d’utilisation et une sécurité optimales. Différents types de plastique existent sur le marché pour satisfaire les exigences des applications et les préférences personnelles : polypropylène (PP) très haute résistance pour les applications en microbiologie ou encore matériaux transparents pour les applications de culture cellulaire de mammifères comme le polycarbonate (PC) ou le polyéthylène téréphtalate glycol (PETG).
Conception : formes spéciales et déflecteurs
L’objectif des cultures agitées est de favoriser l’aération et l’apport en nutriments, tout en empêchant la sédimentation. Les flacons Erlenmeyer traditionnels possèdent une forme conique, caractérisée par une base élargie et un col cylindrique. Ils sont toutefois disponibles dans plusieurs modèles : col large ou étroit, avec ou sans déflecteurs. Des flacons spéciaux sont commercialisés pour favoriser l’échange de gaz, tels que le flacon Fernbach grand volume, avec sa large base offrant une grande surface de transfert d’oxygène, ou les Ultra Yield™ et Optimum Growth Flasks™ à usage unique, dont la géométrie maximise le rapport surface/volume [2].
Avec ou sans déflecteurs : dans les flacons sans déflecteurs, un tourbillon régulier et uniforme se forme, générant un flux bien défini et prévisible [2]. Les cavités au bas des flacons à déflecteurs servent à modifier le tourbillon. En « cassant » le tourbillon, cette conception favorise une meilleure aération et est adaptée aux cultures nécessitant une forte oxygénation. En plus d’améliorer l’aération, les flacons à déflecteurs sont utiles pour les cultures visqueuses, comme les champignons filamenteux, car ils limitent l’agrégation des spores et la formation de culots [3]. D’autre part, le risque de formation de mousse est plus élevé, ce qui peut entraver le transfert d’oxygène. Ainsi, la modification du tourbillon et le flux plus irrégulier font que les flacons à déflecteurs affichent une plus grande variabilité des résultats par rapport aux flacons sans déflecteurs [2].
Matériau : verre ou plastique
Les flacons existent en verre ou en plastique. Pour les applications classiques de microbiologie, les flacons Erlenmeyer en verre, réutilisables et autoclavables, conviennent généralement. Par ailleurs, lorsque le transfert d’oxygène est essentiel, ce matériau hydrophile favorise la formation du film liquide responsable du transfert d’oxygène. En comparaison, le plastique est hydrophobe, sauf traitement spécial [1]. Si toute contamination doit être évitée, par ex. lors de la manipulation de cultures sensibles ou d’étapes de production délicates, les flacons stériles à usage unique équipés d’un capuchon d’aération et d’un filtre de 0,2 µm garantissent une facilité d’utilisation et une sécurité optimales. Différents types de plastique existent sur le marché pour satisfaire les exigences des applications et les préférences personnelles : polypropylène (PP) très haute résistance pour les applications en microbiologie ou encore matériaux transparents pour les applications de culture cellulaire de mammifères comme le polycarbonate (PC) ou le polyéthylène téréphtalate glycol (PETG).
Conception : formes spéciales et déflecteurs
L’objectif des cultures agitées est de favoriser l’aération et l’apport en nutriments, tout en empêchant la sédimentation. Les flacons Erlenmeyer traditionnels possèdent une forme conique, caractérisée par une base élargie et un col cylindrique. Ils sont toutefois disponibles dans plusieurs modèles : col large ou étroit, avec ou sans déflecteurs. Des flacons spéciaux sont commercialisés pour favoriser l’échange de gaz, tels que le flacon Fernbach grand volume, avec sa large base offrant une grande surface de transfert d’oxygène, ou les Ultra Yield™ et Optimum Growth Flasks™ à usage unique, dont la géométrie maximise le rapport surface/volume [2].
Avec ou sans déflecteurs : dans les flacons sans déflecteurs, un tourbillon régulier et uniforme se forme, générant un flux bien défini et prévisible [2]. Les cavités au bas des flacons à déflecteurs servent à modifier le tourbillon. En « cassant » le tourbillon, cette conception favorise une meilleure aération et est adaptée aux cultures nécessitant une forte oxygénation. En plus d’améliorer l’aération, les flacons à déflecteurs sont utiles pour les cultures visqueuses, comme les champignons filamenteux, car ils limitent l’agrégation des spores et la formation de culots [3]. D’autre part, le risque de formation de mousse est plus élevé, ce qui peut entraver le transfert d’oxygène. Ainsi, la modification du tourbillon et le flux plus irrégulier font que les flacons à déflecteurs affichent une plus grande variabilité des résultats par rapport aux flacons sans déflecteurs [2].
Lire la suite
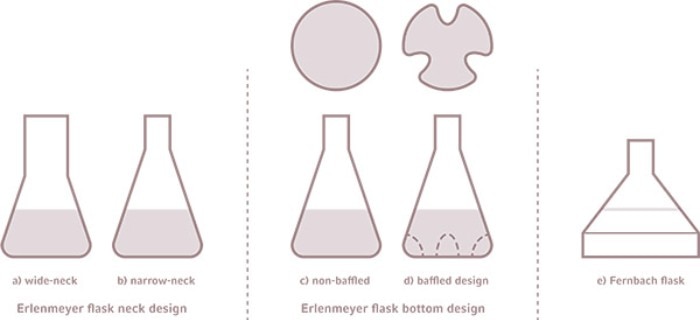
Formes de flacon Erlenmeyer (a) col large (b) col étroit (c) sans déflecteurs (d) avec déflecteurs (e) flacon Fernbach
https://handling-solutions.eppendorf.com/cell-handling/bioprocess/processes-and-applications/detailview/news/its-not-just-about-size-talking-about-shake-flasks-and-bioreactors/
Obturation : traditionnelle avec du coton ou des capuchons d’aération.
Plusieurs types d’obturation existent pour éviter la contamination des cultures. Le rôle de l’obturation est d’éviter la contamination tout en assurant une aération suffisante des cultures. Les solutions d’obturation vont des bouchons traditionnels en passant par des capuchons en métal et des éponges en silicone jusqu’aux capuchons à filtre à usage unique. Le taux de transfert d’oxygène à travers l’obturation dépend du coefficient de diffusion de l’oxygène du matériau, de la largeur du col et de la profondeur du bouchon [1]. Lorsque la contamination constitue un problème, évitez les bouchons en coton, car les projections (par ex. si vous utilisez des flacons à déflecteurs) ou les vapeurs de condensation peuvent humidifier le matériau et provoquer une contamination croisée. Il est généralement déconseillé d’humidifier le haut du col du flacon, non seulement pour réduire la contamination croisée, mais aussi pour ne pas nuire à la perméabilité aux gaz. Cela s’applique également aux matériaux de filtre non hydrophobes pouvant aussi absorber l’humidité. Il est recommandé d’utiliser le même type d’obturation pour les expériences réalisées en parallèle afin d’éviter des variations dans les taux de transfert des gaz.
Recommandations pour les volumes de remplissage
Plus la culture nécessite d’aération, plus le volume de remplissage doit être faible. D’une manière générale, il ne faut pas dépasser 1/5e de la capacité nominale du flacon dans les cultures microbiennes, soit 100 mL pour un flacon Erlenmeyer de 500 mL. Lorsque un transfert d’oxygène maximal est requis, par exemple lors de longues fermentations de souches fortement consommatrices d’oxygène, le volume de remplissage doit être réduit à environ 10 %, tout en augmentant la vitesse d’agitation dans les limites tolérées par la culture en termes de cisaillement. Pour les cultures de cellules de mammifères sensibles au cisaillement, les volumes de remplissage sont généralement plus élevés, de l’ordre de 30 à 40 %, avec une vitesse d’agitation inférieure ou égale à 150 tr/min. Ces dernières années, des flacons spécialement conçus pour l’expression à haut rendement de protéines ou de plasmides, tels que les Ultra Yield™ et Optimum Growth Flasks™ déjà mentionnés, ont été développés. Ils présentent un rapport surface/volume optimisé ainsi que des déflecteurs au fond, ce qui améliore le transfert d’oxygène tout en augmentant le volume de remplissage [2].
Références :
[1] Pauline M. Doran, Bioprocess Engineering Principles (Second Edition), Chapter 10 - Mass Transfer, 2013
[2] htslabs.com
[3] J. Büchs / Biochemical Engineering Journal 7 (2001) 91–98
[4] Filamentous Fungal Cultures – Process Characteristics, Products, and Applications Hesham A. El-Enshasy, in Bioprocessing for Value-Added Products from Renewable Resources, 2007
Obturation : traditionnelle avec du coton ou des capuchons d’aération.
Plusieurs types d’obturation existent pour éviter la contamination des cultures. Le rôle de l’obturation est d’éviter la contamination tout en assurant une aération suffisante des cultures. Les solutions d’obturation vont des bouchons traditionnels en passant par des capuchons en métal et des éponges en silicone jusqu’aux capuchons à filtre à usage unique. Le taux de transfert d’oxygène à travers l’obturation dépend du coefficient de diffusion de l’oxygène du matériau, de la largeur du col et de la profondeur du bouchon [1]. Lorsque la contamination constitue un problème, évitez les bouchons en coton, car les projections (par ex. si vous utilisez des flacons à déflecteurs) ou les vapeurs de condensation peuvent humidifier le matériau et provoquer une contamination croisée. Il est généralement déconseillé d’humidifier le haut du col du flacon, non seulement pour réduire la contamination croisée, mais aussi pour ne pas nuire à la perméabilité aux gaz. Cela s’applique également aux matériaux de filtre non hydrophobes pouvant aussi absorber l’humidité. Il est recommandé d’utiliser le même type d’obturation pour les expériences réalisées en parallèle afin d’éviter des variations dans les taux de transfert des gaz.
Recommandations pour les volumes de remplissage
Plus la culture nécessite d’aération, plus le volume de remplissage doit être faible. D’une manière générale, il ne faut pas dépasser 1/5e de la capacité nominale du flacon dans les cultures microbiennes, soit 100 mL pour un flacon Erlenmeyer de 500 mL. Lorsque un transfert d’oxygène maximal est requis, par exemple lors de longues fermentations de souches fortement consommatrices d’oxygène, le volume de remplissage doit être réduit à environ 10 %, tout en augmentant la vitesse d’agitation dans les limites tolérées par la culture en termes de cisaillement. Pour les cultures de cellules de mammifères sensibles au cisaillement, les volumes de remplissage sont généralement plus élevés, de l’ordre de 30 à 40 %, avec une vitesse d’agitation inférieure ou égale à 150 tr/min. Ces dernières années, des flacons spécialement conçus pour l’expression à haut rendement de protéines ou de plasmides, tels que les Ultra Yield™ et Optimum Growth Flasks™ déjà mentionnés, ont été développés. Ils présentent un rapport surface/volume optimisé ainsi que des déflecteurs au fond, ce qui améliore le transfert d’oxygène tout en augmentant le volume de remplissage [2].
Références :
[1] Pauline M. Doran, Bioprocess Engineering Principles (Second Edition), Chapter 10 - Mass Transfer, 2013
[2] htslabs.com
[3] J. Büchs / Biochemical Engineering Journal 7 (2001) 91–98
[4] Filamentous Fungal Cultures – Process Characteristics, Products, and Applications Hesham A. El-Enshasy, in Bioprocessing for Value-Added Products from Renewable Resources, 2007
Lire la suite

