MENU
PL | PLN
-
-
-
-
- WHX Labs Dubai 2026
- analytica 2026
- Forum Labo 2026
- SLAS Europe 2026
- Forum Labo 2026 Bioprocess
- Bioprocessing Summit Europe 2026
- BioProcess International 2026
- Swiss Biotech Day 2025
- ISCT 2026
- Pichia 2026
- Future Labs Live 2026
- BioProScale Sympposium 2026
- ASGCT 2026
- Eppendorf Automation Forum 2026
- ESACT 2026
-
-
-
-
- WHX Labs Dubai 2026
- analytica 2026
- Forum Labo 2026
- SLAS Europe 2026
- Forum Labo 2026 Bioprocess
- Bioprocessing Summit Europe 2026
- BioProcess International 2026
- Swiss Biotech Day 2025
- ISCT 2026
- Pichia 2026
- Future Labs Live 2026
- BioProScale Sympposium 2026
- ASGCT 2026
- Eppendorf Automation Forum 2026
- ESACT 2026
PL | PLN
-
- Wszystkie wirówki
- Wirówki stołowe
- Wirówki podłogowe
- Wirówki z chłodzeniem
- Mikrowirówki
- Wirówki wielofunkcyjne
- Wirówki wysokoobrotowe
- Ultrawirówki
- Koncentrator
- Wyroby do diagnostyki in vitro
- Materiały zużywalne do wirówek wysokoobrotowych i ultrawirówek
- Probówki wirówkowe
- Płytki wirówkowe
- Oprogramowanie do zarządzania urządzeniami
- Zarządzanie próbkami i informacjami
-
- Wszystkie pipety, dozowniki oraz automatyczne urządzenia do pracy z cieczami
- Pipety mechaniczne
- Pipety elektroniczne
- Pipety wielokanałowe
- Pipety z wyporem bezpośrednim i dozowniki
- Końcówki do pipet
- Dozowniki butelkowe
- Pipetory
- Dozowniki i akcesoria do pipet
- Pipetowanie automatyczne
- Materiały eksploatacyjne do urządzeń automatycznych
- Akcesoria do urządzeń automatycznych
- Systemy do pracy z cieczami i serwisowanie pipet
Sorry, we couldn't find anything on our website containing your search term.
Sorry, we couldn't find anything on our website containing your search term.

Kolby do wytrząsania – tu liczą się nie tylko objętości wypełnienia
Ines Hartmann Akademia laboratoryjna
- Biologia komórki
- Hodowla komórek
- Miksery i wytrząsarki
- Eksperyment
Kultury wytrząsane są hodowane w specjalnych naczyniach, które noszą nazwę kolb Erlenmeyera. W przeciwieństwie do innych naczyń laboratoryjnych, kolby do wytrząsania mają charakterystyczny kształt, który umożliwia dobre wytrząsanie bez rozlewania cieczy. Dowiedz się więcej o różnicach w budowie i materiale oraz ich wpływie na napowietrzanie.
Bioreaktory do wytrząsania - nazywane również kolbami Erlenmeyera - pojawiły się na początku ubiegłego wieku. Dzięki pojemnościom od 25 mL do 5 litrów oferują elastyczność w szerokim zakresie zastosowań badawczych, od badań przesiewowych i ekspansji, po projektowanie pożywek i wczesne etapy opracowywania procesów. Są atrakcyjne cenowo i nadają się do hodowli bakterii, drożdży oraz grzybów, a także komórek roślinnych i zwierzęcych w zawiesinie. Korzystanie z kolb Erlenmeyera nie wymaga wprawdzie specjalnego szkolenia, ale są pewne aspekty, które należy wziąć pod uwagę w celu zapewnienia wydajnej hodowli, a ponadto istnieją różne typy naczyń, które nadają się do różnych zastosowań.
Materiał kolby – szkło kontra plastik
Kolby są dostępne w wersji szklanej lub plastikowej. Do klasycznych zastosowań mikrobiologicznych nadają się w większości przypadków autoklawowalne, wielorazowe, szklane kolby Erlenmeyera. Również wtedy, gdy krytyczny jest transfer tlenu, praca z kolbami szklanymi może być korzystna, ponieważ szkło jako materiał hydrofilowy wspomaga tworzenie się cienkiej warstwy cieczy, który jest odpowiedzialny za transfer tlenu. Z kolei plastik, jeśli nie zostanie poddany specjalnej obróbce, ma właściwości hydrofobowe [1]. W przypadku, gdy zanieczyszczenie odgrywa istotną rolę, np. podczas pracy z wrażliwymi kulturami lub na pewnych etapach produkcji, jednorazowe sterylne kolby z filtrem 0,2 µm oferują najwyższą wygodę i bezpieczeństwo. W zależności od zastosowania i osobistych preferencji na rynku dostępne są różne tworzywa sztuczne. Od wysoce odpornego polipropylenu (PP) do zastosowań mikrobiologicznych po optycznie przezroczyste materiały do hodowli komórek ssaków, takie jak poliwęglan (PC) lub glikol politereftalanu etylenu (PETG).
Konstrukcja kolby – specjalne kształty i przegrody
Celem hodowli wytrząsanych jest zwiększenie napowietrzenia i dostępności składników odżywczych oraz zapobieganie sedymentacji. Typowa kolba Erlenmeyera ma stożkowy korpus z szerszą podstawą i cylindryczną szyjką. Istnieje szereg różnych konstrukcji kolb, z szerokimi lub wąskimi szyjkami, z przegrodami lub bez przegród. Dostępne są konstrukcje specjalne dodatkowo ulepszające wymianę gazową, takie jak kolba Fernbacha dznaczająca się szerszą podstawą i dużą pojemnością, a tym samym dużą powierzchnią do transferu tlenu, czy też jednorazowe kolby Ultra Yield™ i Optimum Growth Flasks™ o zoptymalizowanym kształcie, który pozwala zmaksymalizować stosunek powierzchni do objętości [2].
Z przegrodami czy bez przegród: W kolbach bez przegród tworzy się jednolity, regularny przepływ wirowy cieczy o dobrze zdefiniowanej i przewidywalnej geometrii [2]. Dla porównania w kolbach z przegrodami wir ten jest celowo zakłócany poprzez zastosowanie określonych wgłębień w obszarze dna kolby. Ta „przerywająca wir” konstrukcja poprawia napowietrzanie hodowli i może być korzystna, jeśli hodowla wykazuje wysokie zapotrzebowanie na tlen. Oprócz lepszego napowietrzania, kolby z przegrodami mogą być również przydatne do pracy z lepkimi kulturami, np. grzybami nitkowatymi, ponieważ zapobiegają agregacji zarodników lub osadzaniu się kultury [3]. Z drugiej strony istnieje większe ryzyko tworzenia się piany, która może utrudniać transfer tlenu. Kolby z przegrodami prowadzą również do znacznie bardziej zmiennych wyników niż kolby bez przegród, ze względu na nagłe przerywanie wiru i bardziej chaotyczne zachowanie przepływu [2].
Materiał kolby – szkło kontra plastik
Kolby są dostępne w wersji szklanej lub plastikowej. Do klasycznych zastosowań mikrobiologicznych nadają się w większości przypadków autoklawowalne, wielorazowe, szklane kolby Erlenmeyera. Również wtedy, gdy krytyczny jest transfer tlenu, praca z kolbami szklanymi może być korzystna, ponieważ szkło jako materiał hydrofilowy wspomaga tworzenie się cienkiej warstwy cieczy, który jest odpowiedzialny za transfer tlenu. Z kolei plastik, jeśli nie zostanie poddany specjalnej obróbce, ma właściwości hydrofobowe [1]. W przypadku, gdy zanieczyszczenie odgrywa istotną rolę, np. podczas pracy z wrażliwymi kulturami lub na pewnych etapach produkcji, jednorazowe sterylne kolby z filtrem 0,2 µm oferują najwyższą wygodę i bezpieczeństwo. W zależności od zastosowania i osobistych preferencji na rynku dostępne są różne tworzywa sztuczne. Od wysoce odpornego polipropylenu (PP) do zastosowań mikrobiologicznych po optycznie przezroczyste materiały do hodowli komórek ssaków, takie jak poliwęglan (PC) lub glikol politereftalanu etylenu (PETG).
Konstrukcja kolby – specjalne kształty i przegrody
Celem hodowli wytrząsanych jest zwiększenie napowietrzenia i dostępności składników odżywczych oraz zapobieganie sedymentacji. Typowa kolba Erlenmeyera ma stożkowy korpus z szerszą podstawą i cylindryczną szyjką. Istnieje szereg różnych konstrukcji kolb, z szerokimi lub wąskimi szyjkami, z przegrodami lub bez przegród. Dostępne są konstrukcje specjalne dodatkowo ulepszające wymianę gazową, takie jak kolba Fernbacha dznaczająca się szerszą podstawą i dużą pojemnością, a tym samym dużą powierzchnią do transferu tlenu, czy też jednorazowe kolby Ultra Yield™ i Optimum Growth Flasks™ o zoptymalizowanym kształcie, który pozwala zmaksymalizować stosunek powierzchni do objętości [2].
Z przegrodami czy bez przegród: W kolbach bez przegród tworzy się jednolity, regularny przepływ wirowy cieczy o dobrze zdefiniowanej i przewidywalnej geometrii [2]. Dla porównania w kolbach z przegrodami wir ten jest celowo zakłócany poprzez zastosowanie określonych wgłębień w obszarze dna kolby. Ta „przerywająca wir” konstrukcja poprawia napowietrzanie hodowli i może być korzystna, jeśli hodowla wykazuje wysokie zapotrzebowanie na tlen. Oprócz lepszego napowietrzania, kolby z przegrodami mogą być również przydatne do pracy z lepkimi kulturami, np. grzybami nitkowatymi, ponieważ zapobiegają agregacji zarodników lub osadzaniu się kultury [3]. Z drugiej strony istnieje większe ryzyko tworzenia się piany, która może utrudniać transfer tlenu. Kolby z przegrodami prowadzą również do znacznie bardziej zmiennych wyników niż kolby bez przegród, ze względu na nagłe przerywanie wiru i bardziej chaotyczne zachowanie przepływu [2].
Warto przeczytać
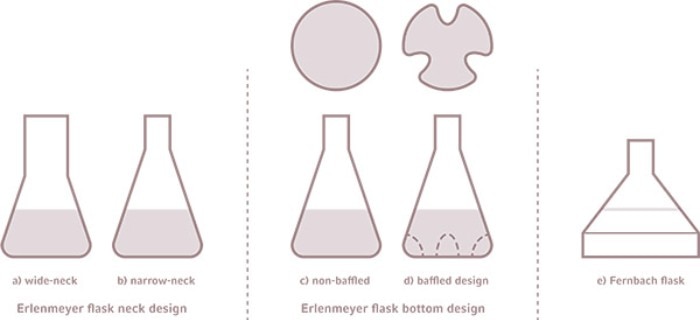
Konstrukcja kolby Erlenmeyera (a) z szeroką szyjką (b) z wąską szyjką (c) bez przegród (d) z przegrodami (e) kolba Fernbacha
https://handling-solutions.eppendorf.com/cell-handling/bioprocess/processes-and-applications/detailview/news/its-not-just-about-size-talking-about-shake-flasks-and-bioreactors/
Zamknięcia kolb - od tradycyjnych bawełnianych po zatyczki wentylowane.
Dostępne są różne zamknięcia kolb zapobiegające zanieczyszczeniu hodowli. Zamknięcie ma zapobiegać zanieczyszczeniu, ale jednocześnie musi umożliwiać wystarczające napowietrzenie kultur. Zamknięcia sięgają od tradycyjnych korków, poprzez metalowe nasadki i silikonowe gąbki, aż po jednorazowe zatyczki z filtrem. Szybkość transferu tlenu przez zamknięcie zależy od współczynnika dyfuzji tlenu w materiale, szerokości otworu szyjki i głębokości korka [1]. Jeśli zanieczyszczenie jest problemem, należy unikać zatyczek bawełnianych, ponieważ wycieki (np. w przypadku użycia kolb z przegrodami) lub para kondensacyjna mogą zwilżyć bawełnę i spowodować zanieczyszczenie krzyżowe. Ogólnie należy unikać zwilżania zamknięcia kolby, nie tylko w celu ograniczenia zanieczyszczenia krzyżowego, ale także aby nie ograniczać przepuszczalności gazu. Dotyczy to również niehydrofobowych materiałów filtracyjnych, które także mogą wchłaniać wilgoć. Do równoległych eksperymentów należy wybierać ten sam typ zamknięcia, aby uniknąć różnych szybkości transferu gazu.
Jakie objętości wypełnienia są zalecane?
Im większe zapotrzebowanie hodowli na napowietrzanie, tym mniejszą objętość wypełnienia należy wybrać. Według ogólnej zasady, w przypadku hodowli mikroorganizmów nie powinno się przekraczać 1/5 nominalnej pojemności kolby, np. 100 mL dla kolby Erlenmeyera o pojemności 500 mL. Jeśli wymagany jest maksymalny transfer tlenu, np. w przypadku długich fermentacji szczepów o wysokim zużyciu tlenu, objętość wypełnienia powinna nawet zostać zmniejszona do 10% przy prędkości obrotowej zwiększonej na tyle, na ile pozwala na to odporność kultury na naprężenia ścinające. W przypadku hodowli ssaczych wrażliwych na ścinanie powszechne są większe objętości wypełnienia w zakresie 30-40%, przy niższych prędkościach wytrząsania ≤ 150 rpm. W ciągu ostatnich lat pojawiły się szczególne typy kolb ukierunkowane na wysoką wydajność ekspresji białek lub plazmidów, na przykład wspomniane wyżej kolby Ultra Yield™ i Optimum Growth Flasks™, obie o zoptymalizowanym stosunku powierzchni do objętości oraz z dolnymi przegrodami dla lepszego transferu tlenu, umożliwiające większą objętość wypełnienia [2].
Bibliografia:
[1] Pauline M. Doran, Bioprocess Engineering Principles (Second Edition), Chapter 10 - Mass Transfer, 2013
[2] htslabs.com
[3] J. Büchs / Biochemical Engineering Journal 7 (2001) 91–98
[4] Filamentous Fungal Cultures – Process Characteristics, Products, and Applications Hesham A. El-Enshasy, in Bioprocessing for Value-Added Products from Renewable Resources, 2007
Zamknięcia kolb - od tradycyjnych bawełnianych po zatyczki wentylowane.
Dostępne są różne zamknięcia kolb zapobiegające zanieczyszczeniu hodowli. Zamknięcie ma zapobiegać zanieczyszczeniu, ale jednocześnie musi umożliwiać wystarczające napowietrzenie kultur. Zamknięcia sięgają od tradycyjnych korków, poprzez metalowe nasadki i silikonowe gąbki, aż po jednorazowe zatyczki z filtrem. Szybkość transferu tlenu przez zamknięcie zależy od współczynnika dyfuzji tlenu w materiale, szerokości otworu szyjki i głębokości korka [1]. Jeśli zanieczyszczenie jest problemem, należy unikać zatyczek bawełnianych, ponieważ wycieki (np. w przypadku użycia kolb z przegrodami) lub para kondensacyjna mogą zwilżyć bawełnę i spowodować zanieczyszczenie krzyżowe. Ogólnie należy unikać zwilżania zamknięcia kolby, nie tylko w celu ograniczenia zanieczyszczenia krzyżowego, ale także aby nie ograniczać przepuszczalności gazu. Dotyczy to również niehydrofobowych materiałów filtracyjnych, które także mogą wchłaniać wilgoć. Do równoległych eksperymentów należy wybierać ten sam typ zamknięcia, aby uniknąć różnych szybkości transferu gazu.
Jakie objętości wypełnienia są zalecane?
Im większe zapotrzebowanie hodowli na napowietrzanie, tym mniejszą objętość wypełnienia należy wybrać. Według ogólnej zasady, w przypadku hodowli mikroorganizmów nie powinno się przekraczać 1/5 nominalnej pojemności kolby, np. 100 mL dla kolby Erlenmeyera o pojemności 500 mL. Jeśli wymagany jest maksymalny transfer tlenu, np. w przypadku długich fermentacji szczepów o wysokim zużyciu tlenu, objętość wypełnienia powinna nawet zostać zmniejszona do 10% przy prędkości obrotowej zwiększonej na tyle, na ile pozwala na to odporność kultury na naprężenia ścinające. W przypadku hodowli ssaczych wrażliwych na ścinanie powszechne są większe objętości wypełnienia w zakresie 30-40%, przy niższych prędkościach wytrząsania ≤ 150 rpm. W ciągu ostatnich lat pojawiły się szczególne typy kolb ukierunkowane na wysoką wydajność ekspresji białek lub plazmidów, na przykład wspomniane wyżej kolby Ultra Yield™ i Optimum Growth Flasks™, obie o zoptymalizowanym stosunku powierzchni do objętości oraz z dolnymi przegrodami dla lepszego transferu tlenu, umożliwiające większą objętość wypełnienia [2].
Bibliografia:
[1] Pauline M. Doran, Bioprocess Engineering Principles (Second Edition), Chapter 10 - Mass Transfer, 2013
[2] htslabs.com
[3] J. Büchs / Biochemical Engineering Journal 7 (2001) 91–98
[4] Filamentous Fungal Cultures – Process Characteristics, Products, and Applications Hesham A. El-Enshasy, in Bioprocessing for Value-Added Products from Renewable Resources, 2007
Warto przeczytać

