메뉴
KR | KRW
KR | KRW
Sorry, we couldn't find anything on our website containing your search term.

셰이크 플라스크 – 단순한 배양 용기 그 이상
Ines Hartmann 실험실 아카데미
- 세포생물학
- Cell Culture
- Mixer 및 Shaker
- 논문
진탕 배양은 Erlenmeyer 플라스크라고도 불리는 특수한 용기에서 이루어집니다. 다른 실험실 용기와 달리, 셰이크 플라스크는 액체가 넘치지 않으면서도 효과적인 진탕이 가능하도록 특수한 형태로 제작됩니다. 이 글에서는 디자인과 재질의 차이와 이러한 차이가 산소 공급에 미치는 영향에 대해 알아봅니다.
셰이킹 바이오리액터는 Erlenmeyer 플라스크 또는 간단히 셰이크 플라스크라고도 하며 지난 세기 초에 도입되었습니다. 25 mL에서 5 L의 용량을 제공하여 스크리닝과 증식부터 배지 디자인과 초기 프로세스 개발에 이르기까지 다양한 실험 목적에 유연하게 활용할 수 있습니다. 셰이크 플라스크는 가격이 경제적이고, 박테리아, 효모, 곰팡이뿐만 아니라 식물 및 동물 세포를 현탁 배양하는 데에도 적합합니다. 셰이크 플라스크는 취급을 위해 특별한 교육이 필요하지 않지만, 효율적인 배양을 위해 고려해야 할 몇 가지 사항이 있고 적용 분야에 따라 적합한 다양한 용기 유형이 존재합니다.
플라스크 재질 – 유리 대 플라스틱
플라스크는 유리나 플라스틱으로 제작됩니다. 전통적인 미생물학 실험에서는 대부분의 경우 재사용할 수 있고 오토클레이브 처리가 가능한 유리 Erlenmeyer 플라스크가 적합합니다. 또한 산소 전달이 중요한 경우에는 유리를 사용하는 것이 유리할 수 있는데, 유리는 친수성 재질로서 산소 전달에 중요한 역할을 하는 액체 막 형성을 효과적으로 지원하기 때문입니다. 이에 반해, 플라스틱은 별도의 처리가 되어 있지 않은 경우 소수성입니다[1]. 오염 관리가 중요한 경우, 예를 들어 민감한 배양액을 다루는 경우나 생산 단계에서는 0.2 µm 필터가 장착된 통기 캡을 갖춘 일회용 멸균 플라스크가 높은 편의성과 안전성을 제공합니다. 플라스틱 플라스크는 적용 분야와 사용자 선호도에 따라 다양한 재질로 제공됩니다. 미생물학 실험에 적합한 내구성이 뛰어난 폴리프로필렌(PP)부터 포유류 세포 배양에 중점을 둔 광학적으로 투명한 폴리카보네이트(PC) 또는 폴리에틸렌 테레프탈레이트 글리콜(PETG)에 이르기까지 다양한 재질이 사용됩니다.
플라스크 디자인 – 특수한 형태와 배플
진탕 배양의 목적은 산소 공급을 증가시키고, 영양분의 이용 가능성을 높이며, 침전을 방지하는 데 있습니다. 일반적인 Erlenmeyer 플라스크는 넓은 바닥을 가진 원추형 몸체와 원통형 목 부분으로 이루어져 있습니다. 넓은 목 또는 좁은 목을 가진 형태, 배플이 있거나 없는 형태 등 다양한 플라스크 디자인이 존재합니다. 또한 기체 교환을 더욱 향상시키기 위한 특수한 디자인의 플라스크도 있습니다. 예를 들어, 바닥이 넓어 산소 전달 면적이 큰 대용량 Fernbach 플라스크나, 표면적 대 부피 비율을 극대화하도록 최적화된 형태로 디자인된 일회용 Ultra Yield™와 Optimum Growth Flasks™가 있습니다[2].
배플 플라스크 대 비배플 플라스크: 비배플 플라스크에서는 균일하고 규칙적이며 기하학적 특성이 명확하고 예측 가능한 소용돌이 형태의 액체 흐름이 형성됩니다[2]. 이에 반해, 배플 플라스크에서는 바닥 부분에 일정한 형태의 캐비티를 적용하여 이러한 소용돌이 흐름을 의도적으로 방해합니다. 이러한 '소용돌이 차단' 디자인은 배양액의 산소 공급을 향상시키고 배양액의 산소 요구량이 높은 경우에 특히 유용합니다. 향상된 산소 공급 외에도, 배플 플라스크는 사상균 등 고점도 배양액을 다룰 때 포자 응집이나 배양액 침전을 방지하는 데 효과적입니다[3]. 반면, 거품 형성의 위험이 높아져 산소 전달을 방해할 수 있습니다. 또한 배플 플라스크는 갑작스러운 소용돌이 방해와 더욱 혼돈스러운 흐름 거동으로 인해 비배플 플라스크에 비해 결과의 변동성이 상당히 크다는 단점이 있습니다[2].
플라스크 재질 – 유리 대 플라스틱
플라스크는 유리나 플라스틱으로 제작됩니다. 전통적인 미생물학 실험에서는 대부분의 경우 재사용할 수 있고 오토클레이브 처리가 가능한 유리 Erlenmeyer 플라스크가 적합합니다. 또한 산소 전달이 중요한 경우에는 유리를 사용하는 것이 유리할 수 있는데, 유리는 친수성 재질로서 산소 전달에 중요한 역할을 하는 액체 막 형성을 효과적으로 지원하기 때문입니다. 이에 반해, 플라스틱은 별도의 처리가 되어 있지 않은 경우 소수성입니다[1]. 오염 관리가 중요한 경우, 예를 들어 민감한 배양액을 다루는 경우나 생산 단계에서는 0.2 µm 필터가 장착된 통기 캡을 갖춘 일회용 멸균 플라스크가 높은 편의성과 안전성을 제공합니다. 플라스틱 플라스크는 적용 분야와 사용자 선호도에 따라 다양한 재질로 제공됩니다. 미생물학 실험에 적합한 내구성이 뛰어난 폴리프로필렌(PP)부터 포유류 세포 배양에 중점을 둔 광학적으로 투명한 폴리카보네이트(PC) 또는 폴리에틸렌 테레프탈레이트 글리콜(PETG)에 이르기까지 다양한 재질이 사용됩니다.
플라스크 디자인 – 특수한 형태와 배플
진탕 배양의 목적은 산소 공급을 증가시키고, 영양분의 이용 가능성을 높이며, 침전을 방지하는 데 있습니다. 일반적인 Erlenmeyer 플라스크는 넓은 바닥을 가진 원추형 몸체와 원통형 목 부분으로 이루어져 있습니다. 넓은 목 또는 좁은 목을 가진 형태, 배플이 있거나 없는 형태 등 다양한 플라스크 디자인이 존재합니다. 또한 기체 교환을 더욱 향상시키기 위한 특수한 디자인의 플라스크도 있습니다. 예를 들어, 바닥이 넓어 산소 전달 면적이 큰 대용량 Fernbach 플라스크나, 표면적 대 부피 비율을 극대화하도록 최적화된 형태로 디자인된 일회용 Ultra Yield™와 Optimum Growth Flasks™가 있습니다[2].
배플 플라스크 대 비배플 플라스크: 비배플 플라스크에서는 균일하고 규칙적이며 기하학적 특성이 명확하고 예측 가능한 소용돌이 형태의 액체 흐름이 형성됩니다[2]. 이에 반해, 배플 플라스크에서는 바닥 부분에 일정한 형태의 캐비티를 적용하여 이러한 소용돌이 흐름을 의도적으로 방해합니다. 이러한 '소용돌이 차단' 디자인은 배양액의 산소 공급을 향상시키고 배양액의 산소 요구량이 높은 경우에 특히 유용합니다. 향상된 산소 공급 외에도, 배플 플라스크는 사상균 등 고점도 배양액을 다룰 때 포자 응집이나 배양액 침전을 방지하는 데 효과적입니다[3]. 반면, 거품 형성의 위험이 높아져 산소 전달을 방해할 수 있습니다. 또한 배플 플라스크는 갑작스러운 소용돌이 방해와 더욱 혼돈스러운 흐름 거동으로 인해 비배플 플라스크에 비해 결과의 변동성이 상당히 크다는 단점이 있습니다[2].
자세히 보기
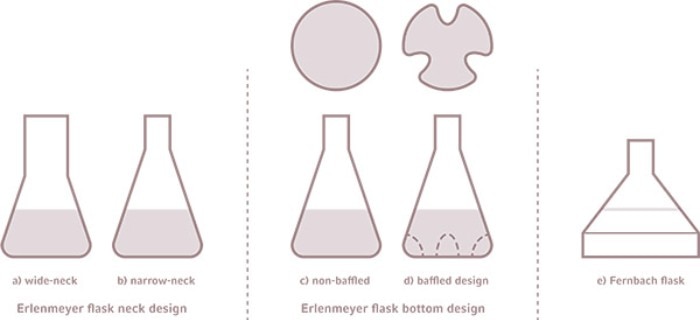
Erlenmeyer 플라스크 디자인 (a) 넓은 목 (b) 좁은 목 (c) 비배플 (d) 배플 (e) Fernbach 플라스크
https://handling-solutions.eppendorf.com/cell-handling/bioprocess/processes-and-applications/detailview/news/its-not-just-about-size-talking-about-shake-flasks-and-bioreactors/
플라스크 마개 – 전통적인 면 마개부터 통기 캡까지
배양액의 오염을 방지하기 위해 플라스크에 다양한 종류의 마개를 사용할 수 있습니다. 마개는 오염을 차단하는 동시에 배양액에 충분한 산소를 공급할 수 있어야 합니다. 플라스크 마개는 전통적인 면 마개부터 금속 캡, 실리콘 스펀지 그리고 일회용 필터 캡까지 다양합니다. 마개를 통한 산소 전달 속도는 마개 재질의 산소 확산 계수, 목 부분의 개구 폭 그리고 마개 깊이에 따라 달라집니다[1]. 오염이 중요한 문제인 경우에는 면 마개의 사용을 피하는 것이 좋습니다. 특히 배플 플라스크 사용 시 액체가 튀거나 응축된 수증기로 인해 면이 젖게 되면 교차 오염이 발생할 수 있습니다. 일반적으로 플라스크 마개가 젖는 것은 교차 오염을 줄이기 위해서뿐만 아니라 가스 투과성이 저하되는 것을 방지하기 위해서도 피해야 합니다. 이는 수분을 흡수할 수 있는 비소수성 필터 재질도 마찬가지입니다. 또한 병렬 실험의 경우 가스 전달 속도의 차이를 방지하기 위해 동일한 종류의 마개를 선택해야 합니다.
권장 충전 부피
배양에서 산소 공급 요구도가 높을수록 충전 부피는 더 낮게 설정해야 합니다. 일반적인 기준으로 미생물 배양의 경우 플라스크의 공칭 용량 대비 1/5을 초과하지 않아야 합니다(예: 500 mL Erlenmeyer 플라스크의 경우 100 mL 이하). 산소 소비량이 많은 균주를 장시간 배양하는 등 최대한의 산소 전달이 필요한 경우에는 충전 부피를 10% 수준까지 낮추고 배양액이 견딜 수 있는 전단 응력 내에서 회전 속도를 최대한 높여야 합니다. 반대로, 전단 응력에 민감한 포유류 세포 배양의 경우에는 30~40%의 높은 충전 부피가 일반적이고, 150 rpm 이하의 낮은 진탕 속도가 사용됩니다. 최근 몇 년간 고수율 단백질 또는 플라스미드 발현을 목표로 한 특수한 플라스크도 개발되었습니다. 앞서 언급한 Ultra Yield™와 Optimum Growth Flasks™는 표면적 대 부피 비율과 바닥 배플이 최적화되어 있어 산소 전달이 더 효율적이기 때문에 더 높은 충전 부피가 가능합니다[2].
참고 자료:
[1] Pauline M. Doran, Bioprocess Engineering Principles (Second Edition), Chapter 10 - Mass Transfer, 2013
[2] htslabs.com
[3] J. Büchs / Biochemical Engineering Journal 7 (2001) 91–98
[4] Filamentous Fungal Cultures – Process Characteristics, Products, and Applications Hesham A. El-Enshasy, in Bioprocessing for Value-Added Products from Renewable Resources, 2007
플라스크 마개 – 전통적인 면 마개부터 통기 캡까지
배양액의 오염을 방지하기 위해 플라스크에 다양한 종류의 마개를 사용할 수 있습니다. 마개는 오염을 차단하는 동시에 배양액에 충분한 산소를 공급할 수 있어야 합니다. 플라스크 마개는 전통적인 면 마개부터 금속 캡, 실리콘 스펀지 그리고 일회용 필터 캡까지 다양합니다. 마개를 통한 산소 전달 속도는 마개 재질의 산소 확산 계수, 목 부분의 개구 폭 그리고 마개 깊이에 따라 달라집니다[1]. 오염이 중요한 문제인 경우에는 면 마개의 사용을 피하는 것이 좋습니다. 특히 배플 플라스크 사용 시 액체가 튀거나 응축된 수증기로 인해 면이 젖게 되면 교차 오염이 발생할 수 있습니다. 일반적으로 플라스크 마개가 젖는 것은 교차 오염을 줄이기 위해서뿐만 아니라 가스 투과성이 저하되는 것을 방지하기 위해서도 피해야 합니다. 이는 수분을 흡수할 수 있는 비소수성 필터 재질도 마찬가지입니다. 또한 병렬 실험의 경우 가스 전달 속도의 차이를 방지하기 위해 동일한 종류의 마개를 선택해야 합니다.
권장 충전 부피
배양에서 산소 공급 요구도가 높을수록 충전 부피는 더 낮게 설정해야 합니다. 일반적인 기준으로 미생물 배양의 경우 플라스크의 공칭 용량 대비 1/5을 초과하지 않아야 합니다(예: 500 mL Erlenmeyer 플라스크의 경우 100 mL 이하). 산소 소비량이 많은 균주를 장시간 배양하는 등 최대한의 산소 전달이 필요한 경우에는 충전 부피를 10% 수준까지 낮추고 배양액이 견딜 수 있는 전단 응력 내에서 회전 속도를 최대한 높여야 합니다. 반대로, 전단 응력에 민감한 포유류 세포 배양의 경우에는 30~40%의 높은 충전 부피가 일반적이고, 150 rpm 이하의 낮은 진탕 속도가 사용됩니다. 최근 몇 년간 고수율 단백질 또는 플라스미드 발현을 목표로 한 특수한 플라스크도 개발되었습니다. 앞서 언급한 Ultra Yield™와 Optimum Growth Flasks™는 표면적 대 부피 비율과 바닥 배플이 최적화되어 있어 산소 전달이 더 효율적이기 때문에 더 높은 충전 부피가 가능합니다[2].
참고 자료:
[1] Pauline M. Doran, Bioprocess Engineering Principles (Second Edition), Chapter 10 - Mass Transfer, 2013
[2] htslabs.com
[3] J. Büchs / Biochemical Engineering Journal 7 (2001) 91–98
[4] Filamentous Fungal Cultures – Process Characteristics, Products, and Applications Hesham A. El-Enshasy, in Bioprocessing for Value-Added Products from Renewable Resources, 2007
자세히 보기

